Die galvanische Oberflächenbeschichtung ist ein Verfahren, bei dem elektrischer Strom Metalle dazu bringt, sich gleichmäßig auf der Oberfläche von Werkstücken abzulagern. Die Metallschicht dient in den meisten Fällen dem Korrosionsschutz, dem Schutz vor mechanischem Verschließ oder der Verbesserung der elektrischen Leitfähigkeit. Außerdem können dekorative Zwecke oder eine leichtere Weiterverarbeitung des Grundmaterials Ziel der galvanisch bewirkten Metallabscheidung sein. Wie das gelingt, soll hier etwas näher erläutert werden.
Was ist Galvanik?
Gleichspannungsquellen aus unterschiedlichen Metallen
Die Bezeichnung Galvanik und die davon abgeleiteten Begriffe gehen auf den italienischen Naturforscher Luigi Galvani zurück, der als erster die Wirkung von elektrischem Strom in einer leitfähigen Flüssigkeit beobachtet hat. Ohne es zu wissen, dass er damit einen Stromkreis aufbaut, hat er zwei unterschiedliche Metalle und einen Froschschenkel durch Drähte miteinander verbunden. Zwischen den unterschiedlichen Metallen hat sich eine elektrische Spannung eingestellt. Als der Stromkreis geschlossen war, ist Strom geflossen und hat den Froschschenkel zum Zucken gebracht. Das Blut im Froschschenkel hat den Strom weitergeleitet.

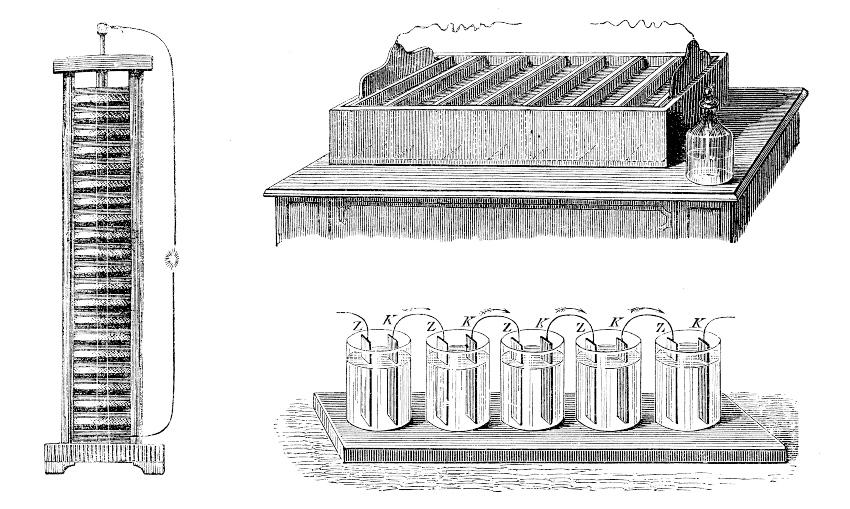
Der Spannungsunterschied zwischen unterschiedlichen Metallen wurde zunächst zur Erzeugung von Gleichstrom in Batterien genutzt. Darin befinden sich Kupfer, Zink und Schwefelsäure. Wird die Batterie in einen geschlossenen Stromkreis eingebaut, liefert sie Strom. Das Zink löst sich dabei nach und nach auf. Wenn es verbraucht ist, ist die Batterie leer.
Galvanische Metallabscheidung
Die galvanische Oberflächenbeschichtung nutzt den entgegengesetzten Vorgang. Eine Gleichspannungsquelle befindet sich in einem geschlossenen Stromkreis, der durch eine leitfähige Flüssigkeit führt. Außerhalb der Flüssigkeit besteht der Strom aus frei beweglichen Elektronen, die vom Minuspol der Spannungsquelle zum Pluspol fließen wollen. Kommen sie in der Flüssigkeit an, wären sie auf eine „Mitfahrgelegenheit“ angewiesen.
Eine einfache „Mitfahrgelegenheit“ gibt es aber nicht. Stattdessen lösen die Elektronen elektrochemische Reaktionen aus. Die Stelle, an der die Elektronen in der Flüssigkeit ankommen, ist die Kathode. Sie zieht die positiv geladenen Metallionen an. Die Metallionen nehmen die Elektronen auf und werden dabei zu einem festen Metall, das sich auf der Kathode absetzt. Das stört das Gleichgewicht zwischen den Metallionen und den negativ geladenen Ionen in der Flüssigkeit. Die negativen Ionen wandern deshalb zu der Stelle, die mit dem Pluspol der Spannungsquelle verbunden ist. Das ist die Anode. Dort liefern sie Elektronen ab. Diese fließen zur Spannungsquelle und der Stromkreis ist geschlossen.
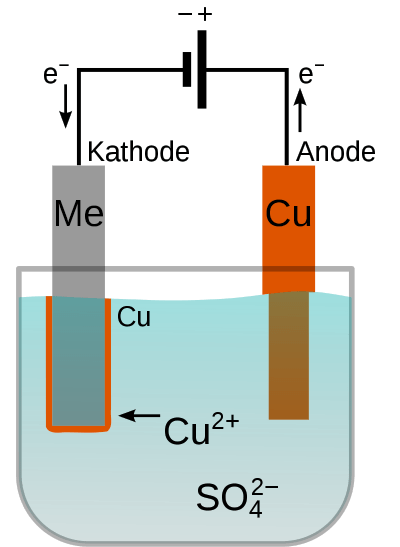
Die Flüssigkeit, in der die elektrochemischen Reaktionen ablaufen, wird als Elektrolyt bezeichnet. Die Beschaffenheit von Anode und Kathode sowie die Zusammensetzung des Elektrolyten bestimmen, welche Reaktionen konkret zustande kommen. Daraus resultieren unterschiedliche elektrochemische Verfahren zur Oberflächenbeschichtung.

Anodische Oxidation
Die galvanische Oberflächenbeschichtung schließt auch chemische Verfahren ein. Dazu zählt die anodische Oxidation, die vor allem für die Herstellung von Schutzschichten auf Aluminium bekannt ist (Eloxieren). Als Elektrolyt dient dabei in der Regel Schwefelsäure, das zu beschichtende Metall wird als Anode geschaltet. Der von außen zugeführte Gleichstrom bewirkt, dass sich an der Anode Sauerstoff abscheidet. Dieser bildet mit dem Grundwerkstoff eine schützende Oxidschicht. Das darunter liegende Metall wird von dieser Beschichtung gleichmäßig bedeckt. Im späteren Einsatz werden Sauerstoff und Feuchtigkeit durch die Oxidschicht von den Oberflächen der behandelten Werkstücke ferngehalten und diese vor Korrosion geschützt.

Metallveredelung ohne äußere Stromquelle
Unedle Metalle lassen sich durch Eintauchen in einen Elektrolyten, der das aufgelöste Salz eines edlen Metalls enthält, galvanisieren. Elektrochemische Prozesse sorgen dafür, dass sich das unedle Metall auflöst und dass sich das edle auf den Oberflächen der Werkstücke abscheidet. Ist die Oberfläche vollständig bedeckt, kommt die Reaktion zum Stillstand.
Das Verhalten unedler Metalle, sich zuerst aufzulösen, wird außer für die galvanische Oberflächenbeschichtung für den aktiven Korrosionsschutz genutzt. Die bekanntesten Beispiele dafür ist das Verzinken von Stahl oder der Einbau von Opferanoden in Schiffsrümpfen. Korrosionsauslösende Faktoren greifen die Zinkschicht oder die Opferanode an und verschonen das Grundmaterial.

Praktische Durchführung der galvanischen Oberflächenbeschichtung
Vor- und Nachbehandlung
Die galvanische Oberflächenbeschichtung funktioniert nur dann zufriedenstellend, wenn die Oberflächen sorgfältig vorbereitet werden. Um eine haltbare Beschichtung aufzubauen müssen die Oberflächen frei von Verunreinigungen sein. Unedle Metallüberzüge (z.B. Zink) benötigen eine Nachbehandlung, bei der eine Konversionsschicht erzeugt (z.B. Phosphatiere, Chromatieren) wird. Vor- und Nachbehandlung sind Verfahrensschritte, die auch in den anderen Bereichen der Oberflächentechnik angewendet werden.
Sollen Kunststoffe oder Glas galvanisiert werden, muss ihre Oberfläche leitfähig sein. Das wird durch die Beschichtung mit metallhaltigem Lack, dünne chemische erzeugte Metallüberzüge oder eine aufwändige Ausstattung mit Metallkeimen erreicht.

Galvanisierung mit Verbrauch der Anode
Die Größe der Werkstücke entscheidet über die Gestaltung der Anlagen, in denen die Beschichtung erzeugt wird. Große Teile werden in Bäder getaucht. Die elektrisch leitende Verbindung zum Minuspol der Gleichstromquelle lässt das Teil zur Kathode werden. Die Anode besteht meistens aus dem Metall, das sich auf der Oberfläche ablagern soll. Als Elektrolyt wird eine Salzlösung eingesetzt, die ebenfalls das Anodenmaterial enthält. Bei geschlossenem Stromkreis wandern die Metallionen zum Werkstück. Gleichzeitig lösen sich aus der Anode Metallionen heraus. Bei guter Badpflege kann dieser Prozess so lange fortgesetzt werden, bis die Anode aufgebraucht ist. Dieses Verfahren wird zum Beispiel für das galvanische Versilbern, Vergolden, Verkupfern und Verzinken eingesetzt.

Galvanisierung mit stabiler Anode
Bei der Beschichtung durch Verchromen enthält nur der Elektrolyt die benötigten Metallionen. An der Anode wird indes Sauerstoff freigesetzt. Dieses Verfahren erfordert eine verstärkte Badkontrolle und die sorgfältige Nachdosierung des Chromsalzes.
Galvanisierung in Trommeln oder Glocken
Die galvanische Oberflächenbeschichtung von Kleinteilen erfolgt in Galvanisiertrommeln oder -glocken. Das sind mit Öffnungen versehende Behälter, die leitend mit dem Minuspol der Spannungsquelle verbunden sind und sich im Elektrolytbad bewegen oder vom Elektrolyt durchspült werden.
Einflussfaktoren auf die Oberflächenbeschichtung
Die Stromstärke entscheidet darüber, wie viel Elektronen an der Kathode zur Verfügung stehen und an der Anode abgeführt werden. Sie ist abhängig von der anliegenden Spannung und der Leitfähigkeit des Elektrolyten. Je höher die Stromstärke ist und je länger sich die Teile im geschlossenen Stromkreis befinden, desto höher wird die Dicke der Metallschicht.

Die Qualität der Beschichtung hängt von der Zusammensetzung und der Temperatur des Elektrolyten ab. Durch Glanzbildner, Netzmittel, pH-Wert Stabilisatoren und andere Hilfsstoffe werden die Eigenschaften der Schicht gezielt beeinflusst. Fremdstoffe, wie Verunreinigungen oder aus den Werkstücken gelöste Ionen stören die galvanische Oberflächenbeschichtung. Deshalb sind die Verwendung von enthärtetem Wasser für den Badansatz und die laufende Badkontrolle entscheidende Voraussetzungen für einen ordnungsgemäßen Schichtaufbau.
 Kluthe Magazin
Kluthe Magazin
